来自Proteopedia
蛋白质组链接蛋白质组链接胸苷酸合成酶(TS)是一种重要的酶单碳代谢TS催化甲基和氢化物从5,10-亚甲基四氢叶酸转移到2-脱氧尿苷-5'-单磷酸盐,从而形成5'-单磷酸胸苷和二氢叶酸。这是人类中dTMP(胸腺嘧啶的前体)的唯一从头来源。[1]
2-脱氧尿苷-5'-单磷酸(dUMP)+5,10-亚甲基四氢叶酸(CH2H(H)4F) ⇌5'-磷酸胸苷(dTMP)+二氢叶酸(H2F)

上图描述了TS催化的整个反应。盒子中的分子部分突出了底物和产物之间的差异。
功能
胸苷酸合成酶使用5,10-亚甲基四氢叶酸作为辅因子催化dUMP甲基化为dTMP。TS对DNA复制和修复至关重要[2]在原生动物中,二氢叶酸还原酶(DHFR)和TS表示为双功能单体酶(DHFR-TS)DHFR实体位于N终端。DHFR和TS催化dTMP生物合成中的连续反应。有两种不同类型的TS–蒂亚和ThyX公司这些类型的活动和结构不同。TS-TyX是黄素依赖酶。
关联
DNA的一个碱基,胞嘧啶,会自发脱氨基形成尿嘧啶,从而改变编码信息。与RNA不同,DNA不含尿嘧啶,而是含有甲基化的胸腺嘧啶,避免了错义突变。这个DNA修复蛋白 尿嘧啶DNA糖苷酶将尿嘧啶识别为受损DNA,将其移除并重新建立原始信息[3]因为胸腺嘧啶含有一个额外的甲基,所以它与尿嘧啶是可以区分的,并且不能通过DNA修复去除。胸苷酸合成酶有助于将丰富的尿苷(含核苷酸尿嘧啶)转化为脱氧胸苷(含核酸胸腺嘧啶),为细胞分裂前的DNA合成做准备。因此,与RNA相比,胸苷酸合成酶在使DNA成为更可靠的遗传信息长期存储中发挥了作用。
叶酸结合部位的TS抑制作用用于抗癌治疗药物。DHFR-TS抑制剂是治疗寄生虫转染疾病的潜在药物靶点。TS表现出类肿瘤活性。[4]
机制
TS的机制可能通过两条潜在的途径发挥作用,但尚不清楚该机制遵循哪条途径。在这两条途径中,底物与酶形成共价三元络合物。这种络合物有助于甲基从CH转移2H(H)4F到dUMP,然后从叶酸基片到dMP基片进行氢化物转移。在A途径中(以红色突出显示),中间复合物仍然与酶共价结合。B途径(以蓝色突出显示)涉及中间体与活性位点半胱氨酸的去耦。

| 结构和配体结合
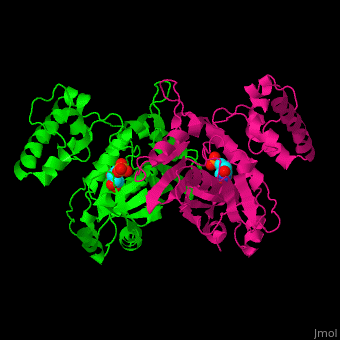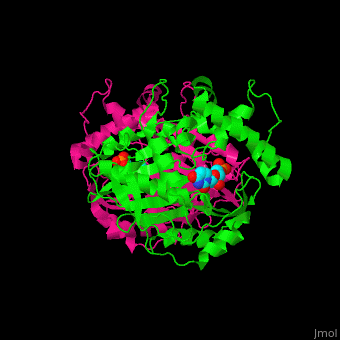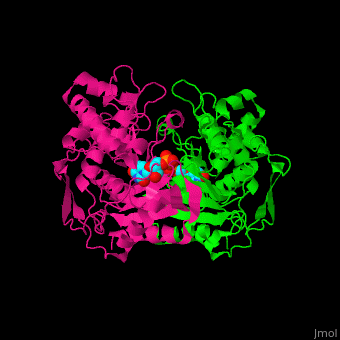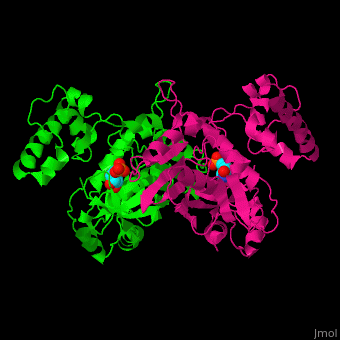
TS形成由两个结构域组成的同型二聚体(重新加载). 他们的每个都能结合底物dUMP吗[5]下图显示了蛋白质和底物之间的一些离子和氢键相互作用,其中大部分也显示在3D场景中。您可以在关闭旋转后测量距离和角度(有关详细说明,请参见查看指南,[1]). 
Maley等人表明,大肠杆菌TS在催化其反应时使用半边机理[6]两个活性位点中的一个催化反应,而另一个保持不活跃。这两个域相互通信以协调这一点的方式仍然未知。 在上述机械假说中,为了区分路径A(半胱氨酸在甲基和氢化物转移过程中保持共价结合)和路径B(半胱胱氨酸对C6的两次亲核攻击),科洛达尔等人将酶与.[1]

天然中间体含有羰基氧(黄色圆圈),而共晶中间体含有胺()而不是在那个位置。在晶体结构测定中,一个活性位点与双底物类似物结合(如图所示),而另一个活性部位与产物结合。这与上面提到的半侧机构相匹配。 活性位点半胱氨酸最初以共价方式与dUMP环的碳6结合。如图所示,中间构象的类似物中所示,它在此处不以共价形式结合。活动部位在结构中无序,显示一种构象显示活性位点半胱氨酸与dMP环的C6碳相距4.21埃,而另一种构象与dMP环的C6碳相距3.84埃。
抑制
甲氨蝶呤是一种竞争性抑制剂,与叶酸底物竞争抑制TS的转化2H(H)4F到H2F.这种抑制阻止产物转化为反应物,阻止细胞繁殖。 下图显示叶酸位于顶部,甲氨蝶呤抑制剂位于底部。比较基板CH2H(H)4F到H2F、 甲氨蝶呤有一个额外的氨基,环中缺少四个氢(即有更多的双键),并且在不同的位置被N-甲基化。 
由于其在细胞分裂中的作用,胸苷酸合成酶已成为抗癌药物的热门靶点。药物5-氟尿嘧啶(5-FU)对胸苷酸合成酶的间接抑制是研究TS功能最常用的抑制剂之一。这种药物间接抑制TS,因为它最终转化为FdUMP,与活性位点半胱氨酸和CH形成共价复合物2H(H)4F.抑制TS可阻止dTMP的生成,并间接阻止2'-脱氧胸腺嘧啶-5'-三磷酸(dTTP)的生成。dTMP和dTTP都是DNA合成的基本构件,它们的缺失会阻碍细胞复制其遗传信息的能力。这对快速分裂并需要大量dTMP和dTTP的癌细胞尤其有效。[7]
|
胸苷酸合成酶的三维结构
胸苷酸合成酶3D结构
致谢
欧肖尼西我想谢谢你Karsten Theis博士还有生物化学II的同学(谢莉·奥尔布赖特,安娜·波斯特尼科娃、和起亚·杨)从2022年春季学期开始,感谢他们对本页的贡献,并感谢马萨诸塞大学阿默斯特分校的克雷格·马丁博士在本页上的反馈。
工具书类
- ↑1 1.1Kholodar SA、Finer-Moore JS、Swiderek K、Arafet K、Moliner V、Stroud RM、Kohen A.《作用中:具有非共价中间类似物的胸腺嘧啶合成酶的X射线结构》。生物化学。2021年4月8日。doi:10.1021/acs.biochem.1c00063。PMID:33829766数字对象标识:http://dx.doi.org/10.1021/acs.biochem.1c00063
- ↑Kaneda S,Nalbantoglu J,Takeishi K,Shimizu K,Gotoh O,Seno T,Ayusawa D.人类胸苷酸合成酶基因的结构和功能分析。生物化学杂志。1990年11月25日;265(33):20277-84. PMID:2243092
- ↑Krokan HE、Drablos F、Slapphaug G.尿嘧啶在DNA中的发生、后果和修复。致癌物。2002年12月16日;21(58):8935-48. doi:10.1038/sj.onc.1205996。PMID:12483510数字对象标识:http://dx.doi.org/10.1038/sj.onc.1205996
- ↑Rahman L、Voeller D、Rahman M、Lipkowitz S、Allegra C、Barrett JC、Kaye FJ、Zajac-Kaye M.胸腺嘧啶合成酶作为癌基因:一种重要DNA合成酶的新作用。癌细胞。2004年4月;5(4):341-51. PMID:15093541
- ↑Finer-Moore JS,Fauman EB,Morse RJ,Santi DV,Stroud RM。盐桥对结合亲和力的贡献和dUMP定向对催化速率的影响:胸腺嘧啶合酶中底物结合精氨酸的突变。蛋白质工程,1996年1月;9(1):69-75. PMID:9053905
- ↑Maley F,Pedersen-Lane J,Changchien L.完全恢复大肠杆菌胸苷酸合成酶非活性突变体的活性:证明大肠杆菌胸磷脂合成酶是一种半边活性酶。生物化学。1995年2月7日;34(5):1469-74. doi:10.1021/bi00005a001。PMID:7849005数字对象标识:http://dx.doi.org/10.1021/bi00005a001
- ↑Costi MP、Ferrari S、Venturelli A、Calo S、Tondi D、Barlocco D。胸苷酸合成酶的结构、功能及其在药物发现中的意义。当前医学化学。2005;12(19):2241-58. doi:10.2174/09298670548668。PMID:16178783数字对象标识:http://dx.doi.org/10.2174/09298670548668